2025.06.14-监管科学大会部分报告分享-附下载地址
中国药品监督管理研究会主办的第八届中国药品监管科学大会在京召开,收集了部分大会的报告,分享给大家。2025.6.14 高天兵副主任-药品检查核查工作最新进展2025.6.14 郭术廷副局长 上海药品监管科学研究与监管实践——以细胞和基因治疗药品全链条质量监管为例2025.6.14 贺伟罡CMDE副主任 监管科学助推医疗器械创新发展2025.6.14 刘继红副司长-深入贯彻全面落实深化药品医疗...
2025年第六期“药审云课堂”-课件和培训视频分享
6月6日CDE进行了2025年度第六期药审云培训,本期以“药品注册申报常见问题”为主题,系统展示药品注册申报流程及多层级多渠道沟通交流机制,让公众更好地了解药品审评工作,同时帮助申请人科学高效推进注册申报进程。课程从资料受理与电子提交、审评期间可能遇到的常见问题与解决路径、核查检验启动工作程序及常见问题解答、临床试验期间安全管理等环节切入,讲解药品注册过程中上述环节的关注要点,同时总结提炼常...
执业药师2025年资料分享-持续更新
我用夸克网盘分享了「执业药师2025」,链接:https://pan.quark.cn/s/fa744764ef3f2025某德培训资料,链接: https://pan.baidu.com/s/1LES35oUPs8ZlBiQI1wg2Vw?pwd=ymth 提取码: ymth
江苏药监局发布《药品生产企业质量安全主体责任指导手册(2.0版)》-附下载地址
为深入贯彻落实《中华人民共和国药品管理法》和全国药品监管工作会议精神,推动药品生产企业全链条压实质量安全主体责任,江苏省药监局于近日正式印发《药品生产企业质量安全主体责任指导手册(2.0版)》,并同步启动全省宣贯实施工作。《指导手册》不仅针对不同药品,如原料药,化学药,生物药,特殊药品精麻,中药配方颗粒等分别制定《指导手册》,而且每个指导手册的内容,是非常的丰富,内容主要包括以下几方面:①...
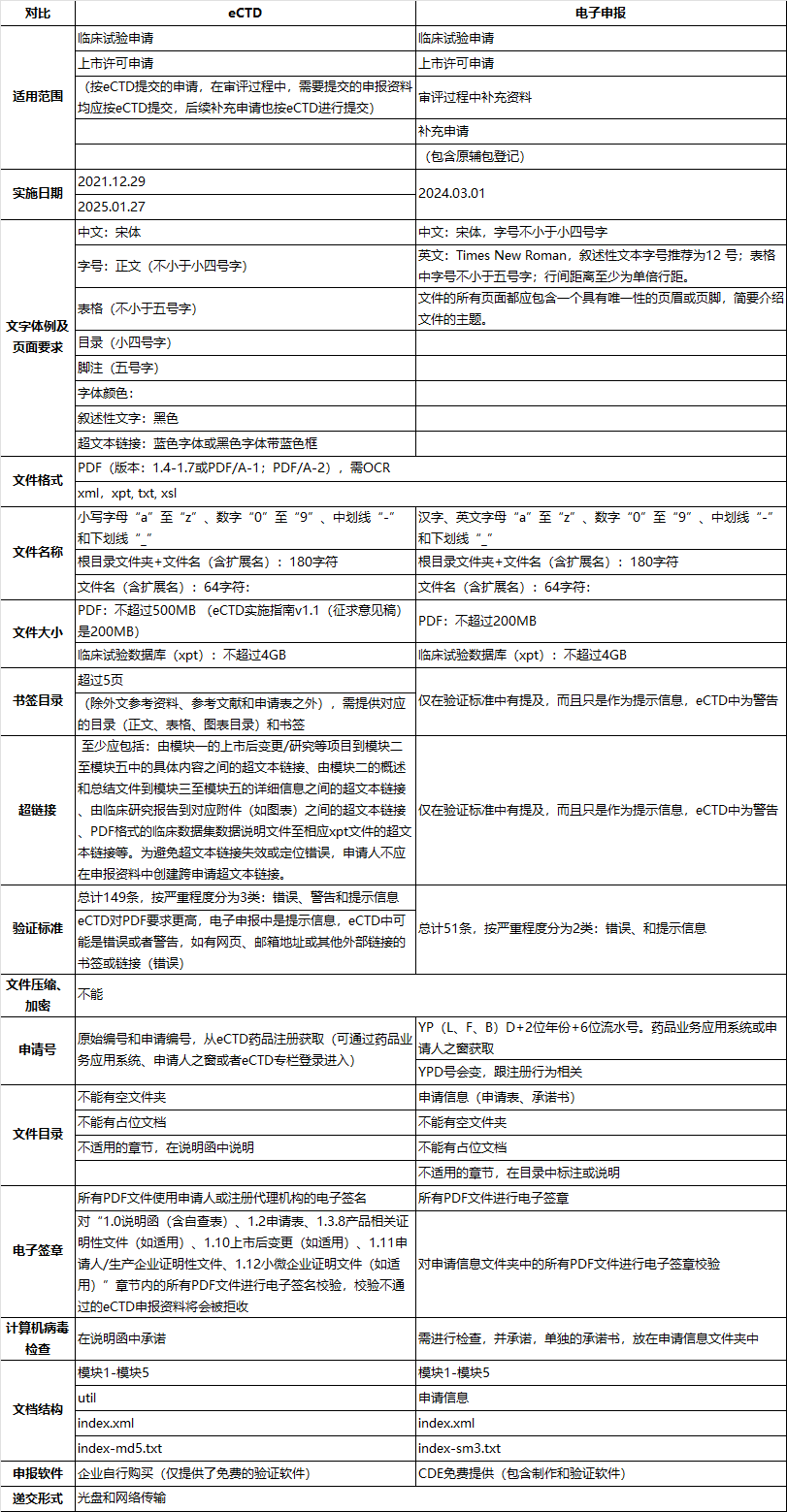
中国eCTD和电子申报差异分析
根据NMPA在2025年1月23日发布的《国家药监局关于扩大药品电子通用技术文档实施范围的公告(2025年第10号)》,自2025年1月27日起,药品电子通用技术文档(eCTD)的实施范围进一步扩大。具体调整如下:1.化学药品:● 化学药品1类至5类的药物临床试验申请;● 化学药品2类、3类、4类、5.2类的上市许可申请2. 生物制品:● 预防用生物制品和治疗用生物制品1类至3类的药物临床试...